[태국] 신규 식품 안전성 평가 지침 공표
태국 비관세장벽 이슈

태국, 신규 식품 관련 지침으로 안전성 평가 의무화
2025년 9월 17일, 태국 식품의약품청(FDA, Food and Drug Administration)은 이전(2023년 6월 27일) 공고를 폐지하고 「식품의약품청 인정 신규 식품(Novel Food) 안전성 평가 기관 및 신규 식품(Novel Food) 안전성 평가 지침」을 새롭게 공표함. 신규 식품을 생산·수입·판매하거나 식품등록번호를 받으려면, 태국 FDA가 승인한 평가기관에서 안전성 평가를 받아야 함
1. 주요 내용
(1) 신규 식품의 범위
① 기존 섭취 이력이 거의 없는 식품: 식품 섭취 이력이 15년 미만인 원료 또는 성분
② 기존과 다른 생산 공정으로 제조된 식품: 성분·구조·형태 등이 변해 영양, 생체 내 화학적 대사, 유해 물질 수준에 영향을 미치는 물질
③ 위의 ① 또는 ②에 해당하는 성분을 포함한 제품
- 식품 첨가물 및 유전자 변형(GMO) 식품은 별도 규정 적용으로 신규 식품 기준에 포함되지 않음
- 구체적 예시로 세포배양육(cell-cultured meat 등)이 신규 식품에 포함되며, 관련 전문 평가기관
(예: 태국 위험 평가 센터, 유전생명공학센터 등)이 담당함
(2) 안전성 평가 기관 및 담당 범위
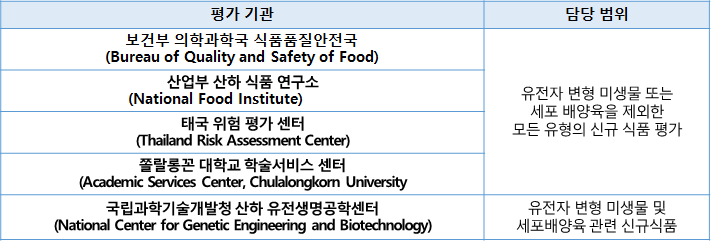
(3) 안전성 평가 절차
① 사전 검토: 제품의 신규 식품 해당 여부를 FDA에 사전 확인 요청 가능, 관련 서류 및 검토 수수료 제출
② 공식 안전성 평가 신청: FDA가 승인한 공인 평가기관에 신청서와 자료 1부 제출
- 평가 신청은 온라인 e-submission 시스템을 통해 전산 제출할 수 있으며, 결과는 신청자와 태국 FDA에 동시에 보고됨
③ 서류 검토 및 보완 요구
④ 전문가 평가 단계: 국제식품규격위원회(Codex)의 화학 물질 위험 평가 지침에 따라 안전성 평가를 진행
- 서류 접수 후 평가 기간은 2~3개월 소요될 것으로 예상
⑤ 결과 보고 및 제출: 평가기관은 안전성 평가보고서를 신청자, FDA에게 제출
(4) 안전성 평가에 필요한 자료
① 식품 일반정보: 학명, 사용 부위, 원산지, 해외 섭취 이력, 제품 구성 및 성분 규격 등
② 안전성 자료: 동물시험 독성자료, 생화학적 특성, 기타 안전성 관련 시험자료
③ 영양정보 및 기능성 정보(선택): 영양성분 프로파일, 건강상 효능 및 관련 연구 결과
④ 해외 평가자료(선택): EU, 일본, 미국 등에서 인정된 신규 식품 평가 결과 첨부 시 심사에 도움이 됨
⑤ 참고 문헌 및 출처
(5) 기타 보완사항
- 세포배양·유전자 변형 식품 관련 품목은 별도 전문 기관을 통해 평가됨
- 신청·등록·결과 처리 등 전 과정은 평가기관-신청자-FDA 간 전산 시스템을 활용해 처리됨
2. 시행일
- 시행일: 2025년 9월 17일
출처
태국 FDA, 『신규 식품 안전성 평가기관 및 평가 지침』, 2025.09.17
식품안전정보원, "태국 식품의약품청, 신소재식품 안전성 평가 기관 및 지침에 관한 식품의약품청 고시 공포", 2025.09.24
'인도,베트남,동남아시아등등' 카테고리의 다른 글
| 베트남 식문화 속에 자리 잡은 K-푸드 (0) | 2025.10.21 |
|---|---|
| 필리핀 음료시장 동향 (0) | 2025.10.21 |
| 파리바게뜨, 몽골 마수걸이 진출…‘고급화·현지화·차별화’ 베이커리 문화 선도 (0) | 2025.10.21 |
| [말레이시아] 11월 1일부터 주류·담배 소비세 인상 (0) | 2025.10.19 |
| [말레이시아] 2026년 예산안 발표(성장과 신중함의 균형) (1) | 2025.10.19 |